Vắc-xin tiêm chủng Việt Nam sử dụng an toàn, hiệu quả
Cập nhật: 25/9/2013 | 8:43:53 PM
Ủy ban Tư vấn toàn cầu về an toàn tiêm chủng kết luận, hiện nay vắc-xin 5 trong 1 của 5 nhà sản xuất khác nhau (trong đó có Quinvaxem Việt Nam sử dụng) đã được WHO tiền thẩm định và khẳng định là an toàn, hiệu quả và đạt chất lượng.
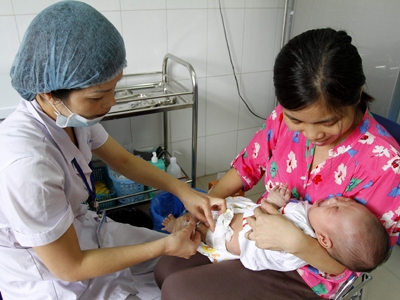
Hiện tượng một số trẻ sơ sinh bị tử vong sau tiêm vắc-xin trong chương trình tiêm chủng mở rộng, đã làm dấy lên những quan ngại về tính an toàn của loại vắc-xin được ngành y tế Việt Nam sử dụng. Ngay sau đó, Bộ Y tế đã tích cực vào cuộc, phối hợp với Tổ chức Y tế thế giới (WHO) và Quỹ Nhi đồng Liên hiệp quốc công bố kết quả đánh giá tính an toàn của vắc-xin Quinvaxem.
Vắc-xin Quinvaxem đã được sử dụng ở hơn 90 nước. Theo WHO, từ năm 2006, vắc-xin Quinvaxem đã được sử dụng ở hơn 90 nước với tổng số trên 400 triệu liều. Từ ngày 1/6/2010, được sự đồng ý của Chính phủ, vắc-xin Quinvaxem đã được đưa vào chương trình Tiêm chủng mở rộng để tiêm chủng cho trẻ em dưới 1 tuổi phòng bệnh bạch hầu, ho gà, uốn ván, viêm gan B và viên phổi/viêm màng não do Hib. Vắc-xin này đã được WHO tiền thẩm định về chất lượng và do Liên minh Toàn cầu về vắc-xin và Tiêm chủng (GAVI) viện trợ cho Việt Nam thông qua UNICEF. Việt Nam đã tiếp nhận 15,8 triệu liều và đã cấp phát 15,2 triệu liều cho các địa phương.
Cuối năm 2012 và đầu năm 2013, Việt Nam đã ghi nhận tần số xuất hiện bất thường của các trường hợp phản ứng sau khi tiêm vắc-xin Quinvaxem. Vì thận trọng và để đảm bảo an toàn hơn cho đối tượng tiêm chủng, đầu tháng 5/2013, Bộ Y tế đã báo cáo Thủ tướng Chính phủ xin phép tạm dừng tiêm vắc-xin Quinvaxem trong tiêm chủng mở rộng, để có thêm thời gian đánh giá một cách toàn diện hơn về nguyên nhân của các phản ứng sau tiêm.
Trong thời gian tạm ngừng sử dụng vắc-xin để đánh giá tính an toàn, Bộ Y tế đã phối hợp với WHO tiến hành một số biện pháp cần thiết như sau: Làm việc với nhóm chuyên gia hàng đầu của WHO để đánh giá tất cả các trường hợp phản ứng sau tiêm đồng thời gửi mẫu vắc-xin các lô có nghi ngờ liên quan đến phản ứng cho đơn vị kiểm định độc lập là Viện Kiểm định Chuẩn thức quốc gia vắc-xin, sinh phẩm y tế Vương quốc Anh; làm việc với nhà sản xuất vắc-xin Quinvaxem ở Triều Tiên để xem xét các loại giấy tờ có liên quan đến việc sản xuất vắc-xin; mời Ban tư vấn toàn cầu xem xét lại các trường hợp nghi có tai biến liên quan đến trường hợp có sử dụng vắc-xin sau đó tham dự và thảo luận về các trường hợp phản ứng sau tiêm ở Việt Nam tại Hội nghị của Ủy ban Tư vấn toàn cầu về an toàn tiêm chủng tại Geneve, Thụy Sĩ ngày 12/6/2013.Qua đánh giá của các chuyên gia hàng đầu của WHO đối với tất cả các trường hợp phản ứng nặng, tử vong sau tiêm vắc-xin Quinvaxem, từ năm 2010 đến nay cho thấy trong số 43 trường hợp nặng có 27 trường hợp tử vong đều không liên quan đến tiêm chủng. Có 9 trường hợp có thể coi là có liên quan đến vắc-xin Quinvaxem nhưng đều hồi phục. Các trường hợp còn lại được xác định không liên quan đến tiêm chủng và chất lượng vắc-xin.
Từ đầu năm 2013 trở lại đây có 5 trường hợp tử vong sau tiêm vắc-xin Quinvaxem, theo đánh giá của nhóm chuyên gia đều không liên quan đến tiêm chủng và chất lượng vắc-xin. Đoàn chuyên gia đánh giá đã nhận định không có bất kỳ dấu hiệu nào liên quan đến tính an toàn của vắc-xin và kỹ thuật tiêm chủng vì các bằng chứng lâm sàng không cho thấy cơ chế bệnh lý chung đối với các trường hợp này.Ngày 12/6/2013 tại Genève, Ủy ban Tư vấn toàn cầu về an toàn tiêm chủng đã tổ chức cuộc họp gồm hơn 30 chuyên gia hàng đầu về tiêm chủng đã xem xét tất cả các trường hợp phản ứng nặng sau tiêm vắc-xin 5 trong 1, trong đó có Việt Nam, và nhận định không có bằng chứng về các trường hợp phản ứng sau tiêm chủng nặng, tử vong liên quan tới việc sử dụng vắc-xin.
Ủy ban tư vấn toàn cầu kết luận: “Vắc-xin 5 trong 1 mang lại lợi ích rất to lớn cho y tế công cộng trong việc bảo vệ 5 bệnh phổ biến ở trẻ em chỉ với một mũi tiêm. Hiện nay vắc-xin 5 trong 1 của 5 nhà sản xuất khác nhau (trong đó có Quinvaxem) đã được WHO tiền thẩm định và khẳng định là an toàn, hiệu quả và đạt chất lượng”.
Kết quả kiểm định độc lập của Viện Kiểm định chuẩn thức Quốc gia vắc-xin và sinh phẩm y tế Vương quốc Anh cũng cho biết: mẫu vắc-xin Quinvaxem thuộc 3 lô 1453037, 1453074 và 1453127 - các lô vắc-xin có nghi ngờ liên quan đến phản ứng nặng sau tiêm tại Việt Nam đã được kiểm định chất lượng tại phòng xét nghiệm độc lập thuộc viện. Kết quả kiểm định ngày 14/6/2013 cho thấy các lô vắc-xin nói trên đạt các yêu cầu về chất lượng.Ngày 17/6/2013, WHO có công văn gửi Bộ Y tế và Bộ Ngoại giao khẳng định vắc-xin Quinvaxem đạt yêu cầu về chất lượng, an toàn, hiệu quả và khuyến cáo rằng vắc-xin này phù hợp để sử dụng trong các chương trình tiêm chủng Quốc gia.
Căn cứ các kết quả của WHO vừa công bố và kinh nghiệm của các nước đã sử dụng lại vắc-xin Quinvaxem sau một thời gian tạm dừng (như Sri Lanka, Bhutan), căn cứ kết luận của Hội đồng Tư vấn sử dụng vắc-xin, sinh phẩm y tế, GS.TS Nguyễn Trần Hiển, Viện trưởng Viện Vệ sinh dịch tễ Trung ương, Trưởng ban quản lý Dự án tiêm chủng mở rộng cho biết, vắc-xin Quinvaxem đã được WHO công nhận đạt yêu cầu về chất lượng, an toàn, hiệu quả và khuyến cáo rằng vắc-xin này phù hợp để sử dụng trong các chương trình tiêm chủng Quốc gia.
(Nguồn: suckhoedoisong.vn)
- Nhu cầu mua vacxin dịch vụ cho Trung tâm Kiểm soát bệnh tật Quảng Ninh (15/7/2024)

- V/v Thẩm định giá: Lô máy móc tài sản, trang thiết bị công nghệ kỹ thuật lạc hậu, hư hỏng, hết khấu hao, không còn khả năng sử dụng, không sửa chữa được của Trung tâm Kiểm soát Bệnh tật tỉnh Quảng Ninh năm 2024 (15/7/2024)

- V/v mời tham gia khảo sát lập phương án và báo giá thực hiện cải tạo bổ sung Hệ thống PCCC tại các đơn vị y tế trực thuộc Sở Y tế (15/7/2024)

- Đoàn công tác CDC Điện Biên đến tham quan, học tập, trao đổi kinh nghiệm tại CDC Quảng Ninh (12/7/2024)

- Nhu cầu lắp đặt vách trang trí phòng họp (12/7/2024)

- Nhu cầu cung cấp phụ tùng và sửa chữa Xe ô tô Toyota Hilux (12/7/2024)

- Nhu cầu quay, chụp toàn cảnh đơn vị theo phần mềm thực tế ảo VR360 (12/7/2024)
- Tập huấn công tác Bảo vệ môi trường y tế năm 2024 (12/7/2024)

- Tháng 10, đồng loạt tiêm lại vắc-xin Quinvaxem (25/9/2013)
- Phòng chống dịch cúm A trên người: Không thể chủ quan, lơ là (25/9/2013)
- Đau mắt đỏ lây truyền ”chóng mặt” qua đường hô hấp (25/9/2013)
- Thấp thỏm sử dụng lại vắc xin Quinvaxem (25/9/2013)
- Tiêm vaccin cho muỗi - Xóa sổ bệnh sốt rét và sốt xuất huyết (24/9/2013)
- Đại dịch AIDS sẽ chấm dứt vào năm 2030 (24/9/2013)
- Dịch đau mắt đỏ lan rộng, ’cháy’ thuốc điều trị (23/9/2013)
- Báo động dịch virus Tây sông Nile lan rộng tại Serbia (21/9/2013)
- Hà Nội bùng phát dịch đau mắt đỏ (19/9/2013)
- Bộ Y tế, Bộ GD-ĐT bất đồng về đào tạo bác sĩ (18/9/2013)
- Tiêu điểm nóng
- Tin đọc nhiều